INTRODUCTION
인두염은 가정의학과 및 소아과에서 가장 흔하게 접하는 질환 중 하나로서[1] 주로 rhinovirus 등 바이러스 감염에 의해 발생하며, 약 10-20%는 세균 감염이 원인이다[2,3]. A군 사슬알균은 세균 성 인두염의 가장 흔한 원인으로서 특히 5-15세에 흔하며[4,5] 소아 인두염의 20-30%, 성인 인두염 의 5-15%와 연관된다[2,6,7]. 소아에서의 A군 사슬알균 인두염을 증상과 진찰 소견만으로 진단하 는 것에 대한 많은 연구들이 있지만 5가지 증상(성홍열성 발진, 구개의 점상출혈, 인두의 화농성 삼출액, 구토, 경부임파절 압통)이 50% 이상에서 연관은 되나 이러한 진찰 소견만으로는 A군 사 슬알균 인두염을 정확히 진단할 수 없다[4]. A군 사슬알균에 의한 인두염은 바이러스성 인두염에 비해 증상이 심하고 화농성(편도주위농양, 후인두농양, 임파절염) 및 비화농성(급성사구체신염, 류마티스열) 합병증[8]을 초래할 수 있기 때문에 정확한 진단과 항생제 치료가 중요하다[9]. A군 사슬알균 인두염을 정확하고 신속하게 진단하는 것은 바이러스 인두염에 대한 불필요한 항생제 의 남용을 막고 세균성 인두염에는 신속하게 항생제를 투여하여 증상 지속 기간을 줄이고 합병 증을 막으며 주변 사람에게 전염력을 낮추는 등의 효과를 나타내므로 매우 중요하다.
전통적인 세균배양법은 A군 사슬알균을 확인하는 표준검사법으로서[9] 이 검사를 시행하기 위해서는 미생물 검사실의 기본 설비와 숙련된 검사자의 기술이 필요하며 균을 동정하는데 최소 하루에서 이틀의 시간이 소요되므로 개인 의원이나 소규모 병원에서 일상적으로 시행하기는 어 렵다. 또한 세균배양법의 민감도는 90-95%로 알려져 있다[10]. 이러한 세균배양의 단점을 보완하 기 위해 10분 이내에 결과 확인이 가능한 신속항원검사가 개발되었고, 초기의 낮은 민감도가 개 선된 새로운 제품이 개발되고 있다[11-13].
이에 저자들은 A군 사슬알균 진단에 면역형광법으로 개발된 STANDARD F Strep A Ag FIA (SD BIOSENSOR, Suwon, Korea) 신속항원검사 제품의 성능을 평가하고자 배양검사와 결과를 비교하 였고, 기존의 신속항원검사로 Sofia Strep A FIA (Quidel, San Diego, CA, USA) 검사를 동시에 시행 하여 결과의 일치도를 평가하였다.
MATERIALS AND METHODS
대상
2018년 7월부터 2019년 10월까지 창원지역 5개의 소아과의원에 내원한 환자들 중 A 군 사슬알 균 인두염이 의심되는 환자 총 372명을 대상으로 하였다. 환자의 편도에서 3개의 검체를 채취하 여 2개의 검체는 상품화 된 STANDARD F Strep A Ag FIA 검사와 Sofia Strep A FIA 검사를 설명서 대로 즉시 수행하였고, 나머지 1개의 검체는 창원경상대학교병원으로 운송하여 인두배양검사를 시행하였다. 임상시험을 시작하기 전 창원경상대학교병원 임상심의위원회(IRB)로부터 승인을 획득한 후 연구를 진행하였고, 참여한 대상자 혹은 보호자에게 모두 서면동의서를 받았다(IRB No. GNUCH 2018-06-011).
신속항원검사
STANDARD F Strep A Ag FIA 검사는 제조사의 지침에 따라 진행하였다. 추출 완충용액 1 튜브 에 추출 완충용액 2를 3방울 떨어뜨린 후 면봉을 이용하여 편도 표면을 문지른 후 검체를 채취한 면봉을 튜브에 넣어 1분간 방치한 뒤, 면봉을 바닥과 벽 쪽으로 10회 이상 문지른 다음 면봉을 제 거하였다. 피펫으로 검체 100 μL를 시험 디바이스에 분주하고 STANDARD F200 분석장비(SD BIOSENSOR)를 이용하여 결과를 판독하였다.
Sofia Strep A FIA 검사는 제조사의 지침에 따라 검사를 진행하였다. 먼저 시약 용액병을 잡고 안 에 있는 앰플용 유리병을 깬 뒤 용기를 다섯번 흔들어 혼합용액이 녹색이 되는 것을 확인하고, 뚜 껑을 열어 수직으로 세워 시약튜브에 혼합 용액을 표시선까지 약 6방울 넣었다. 검체를 채취한 면 봉을 시약튜브에 넣고 위아래로 혼합한 후 1분간 방치하였다. 면봉을 제거하고 피펫으로 100 μL 를 시험 디바이스에 분주하고 Sofia 형광면역장비(Quidel)를 이용하여 결과를 판독하였다.
배양검사
검체를 채취한 면봉을 혈액한천 배지에 접종하고 반정량법으로 집락 수를 측정하였다. 1차 분 획 부위에 bacitracin disk (0.04 U)를 놓고, 37°C 배양기에서 16-18시간 배양하였다. 완전 용혈을 보 이는 집락이 있는지 관찰하고, 해당 집락이 bacitracin disk에 감수성을 보이는지 확인하는 동시에 MALDI-TOF MS (bioMérieux SA, Marcy L’Étoile, France)를 이용하여 A군 사슬알균을 동정하였다.
통계 분석
통계분석은 SPSS 22.0 for Windows (SPSS Inc., Chicago, IL, USA) 프로그램을 이용하였다. STANDARD F Strep A Ag FIA 검사와 인두배양결과를 기준으로 하여 Pearson's chi-ssquare 검정을 이용하였고 P값이 0.05 미만을 통계적으로 유의한 것으로 정의하고 이를 바탕으로 민감도, 특이 도, 양성예측도, 음성예측도를 산출하였다. 신속항원 검사간 일치도 평가를 위하여 양성 일치율, 음성 일치율, 전체 일치율 및 Cohens kappa를 계산하였고, 그 값에 따라 (0.01-0.20, slight agreement; 0.21-0.40, fair agreement; 0.41-0.60, moderate agreement; 0.61-0.80, substantial agreement; 0.81-0.99, almost perfect agreement) 해석하였다.
RESULTS
STANDARD F Strep A Ag FIA와 배양검사 간의 비교
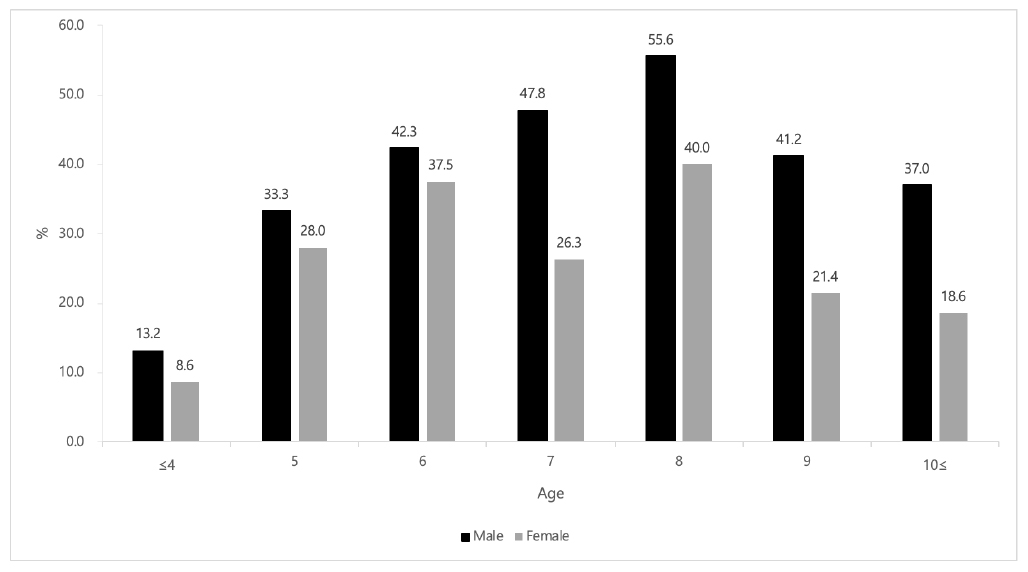
STANDARD F Strep A Ag FIA 검사와 배양검사를 동시에 시행한 372 검체 중 배양검사 양성은 101 검체, 음성은 271 검체, STANDARD F Strep A Ag FIA 검사 양성은 109 검체, 음성은 263 검체 였다(Table 1). 총 372 검체에 대해 배양검사를 기준으로 하였을 때 STANDARD F Strep A Ag FIA 검사의 민감도는 95.0% (95% 신뢰구간 88.8-98.4%), 특이도는 95.2% (95% 신뢰구간 91.9-97.4%) 였고, 양성예측도는 88.1% (95% 신뢰구간 80.5-93.5%), 음성예측도는 98.1% (95% 신뢰구간 95.6- 99.4%)였다. 연령별 양성률은 8세가 47.8%로 가장 높았고, 6세 39.9%, 7세 37.1% 였으며, 남자는 57.8%, 여자는 42.2%였다(Fig. 1).
Table 1
Clinical performance of STANDARD F Strep A Ag FIA and Sofia Strep A FIA compared to throat culture
신속항원검사 간의 일치도 비교
STANDARD F Strep A Ag FIA 검사와 Sofia Strep A FIA 검사결과를 종합하여 두 의료기기 간 의 일치도를 평가하였다. 양성 일치율은 92.7% (95% 신뢰구간 86.1-96.8%), 음성 일치율은 98.1% (95.6-99.4%), 전체 일치율은 96.5% (95% 신뢰구간 92.8-97.3%)를 나타내었고 Cohens kappa 값은 0.89 (95% 신뢰구간 0.84-0.94%)를 나타냈다.
배양검사와 두 신속항원검사의 결과 비교
배양검사와 두 신속검사의 결과를 비교했을 때 배양검사와 STANDARD F Strep A Ag FIA 두 가 지 모두 양성이고 Sofia Strep A FIA 검사만 음성인 경우는 2개 검체였고, 배양검사와 Sofia Strep A FIA 검사가 모두 양성이고 STANDARD F Strep A Ag FIA 검사만 음성인 경우는 1개 검체였다. 배 양검사는 양성인데 두 신속항원 결과가 모두 음성을 나타낸 경우는 4개 검체였고, 배양검사는 음 성인데 STANDARD F Strep A Ag FIA 양성인 경우는 13개인 반면, Sofia Strep A FIA 양성인 경우는 11개였다. 7개의 검체에서는 배양검사는 음성인데 두 신속 항원검사에서 모두 양성을 나타냈다.
DISCUSSION
A군 사슬알균 신속항원검사는 검사 방법이 간편하고 검사 시간이 10분 이내로 짧아 환자가 병 원에 여러 번 내원할 필요없이 의사의 진찰과 검사만으로 세균성 인두염의 진단과 처방이 가능 하므로 진료에 매우 유용하다. 또한 A군 사슬알균은 세균성 인두염의 가장 흔한 원인으로 대부분 페니실린에 감수성을 나타내므로 세균배양검사 없이 신속항원검사만으로 진단과 치료가 가능 하다. 하지만 세균성 인두염이 의심되는 환자에서 A군 사슬알균 신속항원검사가 음성인 경우나 페니실린에 잘 치료되지 않아 항균제 감수성 결과가 필요한 경우에는 배양검사를 추가로 시행해 야 한다[1].
A군 사슬알균 인두염을 진단하기 위한 신속항원검사는 1980년대부터 개발되기 시작하여 점 차 그 성능이 개선되고 있으며, 검사 원리는 면역법에서 분자유전법에 이르기 까지 다양하다. 본 연구에서 평가한 STANDARD F Strep A Ag FIA 검사는 사람의 인후 검체에 있는 A군 사슬알균 의 항원을 면역크로마토그래피법으로 감지하여 형광으로 정성 검출하는 의료기기로서 기존의 인두 배양검사와 비교하여 높은 민감도(95%)를 나타냈으며 이는 다른 연구들에서 메타분석으 로 보고되는 신속항원검사의 민감도(86%)보다 월등히 높았다[3,14]. 다른 신속항원검사인 Sofia Strep A FIA 검사와의 일치도는 96.5%, kappa 0.89로 '거의 완벽한 일치' 수준을 나타냈다. 따라서 인두염 의심 환자에서 선별검사로 STANDARD F Strep A Ag FIA 검사를 사용하면 세균성 인두염 의 진단에 유용할 것으로 생각된다.
STANDARD F Strep A Ag FIA 검사는 특이도(95.2%)가 높아 바이러스성 인두염에 대한 불필요 한 항균제 처방을 줄일 수 있으며 이는 전체 진료비 절감에도 유용할 것이다. 인두염 의심 소아를 대상으로 진행한 관찰 연구에 따르면 신속항원검사를 시행하기 전에는 80%의 환자에게 경험적 항균제를 처방한 반면, 신속항원검사를 시행하고 그 결과에 따라 항균제를 처방하였을 때는 37% 의 환자에서만 항균제를 처방하였고 76%의 진료비용 감소를 나타냈다고 한다[15].
인두염의 치료 전략에 사용되는 modified Centor 스코어(McIsaac) 기준에서는 스코어(각 1점 산 정; 24시간 지속되는 열, 심한 염증성의 편도, 기침이나 코감기 없음, 증상 발현 3일 이내, 화농성 편도)가 0 혹은 1 이면 신속항원검사나 항균제 치료를 권장하지 않으며, 3-15세 환자에서 스코 어 1 인 경우와 스코어 2와 3 의 경우 세균성 감염과 바이러스성 감염의 감별을 위해 신속항원검 사 혹은 배양검사를 시행하도록 하고 있다. 또한 스코어 4의 경우 A군 사슬알균 인두염일 확률 이 50% 이상으로 경험적 항생제의 사용을 고려할 수 있다[16,17]. 미국감염학회와 가정의학회에 서는 소아에서 세균성 인두염이 의심될 때 신속항원검사를 먼저 시행하고 그 결과가 양성이면 항균제 치료를 시행하도록 권장하고 있다[7,18]. 우리나라에서는 A군 사슬알균 신속항원검사나 modified Centor 스코어 등을 아직 진료에 널리 활용하고 있지는 않지만, 근거중심의 진료 문화가 자리잡고 항생제 오남용에 대한 환자 및 사회적 경각심이 높아짐에 따라 인두염 의심 환자의 진 료 시 신속항원검사를 시행하는 것에 대한 의사와 환자의 자발적인 수요는 점차 증가할 것으로 생각된다. 더 나아가 진료에 유용한 이러한 검사의 사용은 정확한 진단과 치료를 위한 당위적인 의료의 질 개선의 한 부분으로 새로운 검사에 대한 진료의사의 인식이 개선되고 검사에 대한 접 근성이 용이해야 한다. 이를 위해서는 진단검사의학회 차원에서의 검사 홍보나 진료지침 개발이 필요하며 해당 진료과의 진료지침에도 반영될 수 있도록 적극 힘써야 할 것이다.
반면 신속항원검사는 임상적 사용에 있어 몇 가지 주의를 요한다. 먼저 신속항원검사 단독으 로는 A군 사슬알균의 보균자와 감염자를 구분할 수는 없으며 이것은 세균배양법도 마찬가지이 다. 무증상 보균자는 신속항원검사에 양성이지만 항균제 처방이 불필요하며 정상 학동기 소아의 무증상 A군 사슬알균 보균율은 약 10% 정도로 알려져 있다[2]. 또한 검사에 영향을 미치는 여러 가지 내외적 요인들에 대한 이해가 필요하다. 예를 들어 검사 기기나 원리별 민감도 차이, 검사를 시행하는 검사자의 기술 숙련도, 검체의 수집/운반/저장, 환자의 항균제 투여나 질병의 진행 경과, 그리고 A군 사슬알균 인두염의 유병률 등이 이에 해당한다[19-21]. 즉, 신속항원검사의 기기가 다 르거나 검사법의 차이로 인한 결과 불일치에 대해 분자유전법으로 확인이 필요할 수 있고, 검사 실에서는 지침에 따른 일관된 검사수행으로 검사자 요인의 간섭에 대한 배제가 필요하다. 또한 정확한 검체 채취는 검사 결과에 영향을 미치는 가장 중요한 과정으로 편도 부위를 비교적 세게 여러 번 문질러야 하며 채취한 면봉이 구강 내 다른 부위에 닿지 않게 주의해야 한다. 검체 채취 후 검사실로의 운반은 빠를수록 좋으며 장시간의 운반을 위해서는 수송배지를 사용하고 적정온 도를 유지해야 한다. 이와 같은 검체 채취자의 검사에 대한 이해와 검체 채취 및 운송에 대한 지식 은 실제 진료 현장에서는 간과하기 쉬운 부분이지만 결과에 미치는 영향은 매우 크다[22]. 환자의 상태 또한 검사 결과를 해석하는데 중요하며, 항균제 치료를 받은 경우 배양검사 결과가 음성일 수 있다. 본 연구에서는 이에 대한 요인들을 분석하지 못하였지만, 다양한 요인들에 의해 세 가지 검사 결과에 차이가 났다고 예상할 수 있다. 특히 면봉으로 세 번이나 검체를 채취하므로, 검체마 다 채취되는 균 수가 차이가 날 수 있다.
결론적으로 STANDARD F Strep A Ag FIA는 A군 사슬알균 인두염에 대한 신속항원검사로서 표준 검사법인 배양검사와 비교했을 때 민감도와 특이도가 높고, Sofia Strep A FIA 신속항원검사 와 거의 완벽한 일치를 나타내므로 증상만으로 원인 감별이 어려운 소아 인두염 환자의 빠른 진 단과 항균제 사용 결정에 도움이 될 수 있을 것이다. 이에 저자들은 진료의사들이 인두염 환자를 진료할 때 A군 사슬알균 신속항원검사를 적극 활용해 주기를 바란다.