Department of Laboratory Medicine, Inje University College of Medicine, Busan, Korea
Corresponding to Sae Am Song, E-mail: songsaeam@paik.ac.kr
Ann Clin Microbiol 2022;25(3):67-72. https://doi.org/10.5145/ACM.2022.25.3.1
Received on 4 August 2022, Revised on 11 August 2022, Accepted on 11 August 2022, Published on 20 September 2022.
Copyright © Korean Society of Clinical Microbiology.
This is an Open Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (https://creativecommons.org/licenses/by-nc/4.0/) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
Clinical and Laboratory Standards Institute and European Committee on Antimicrobial Susceptibility Testing (EUCAST) clinical breakpoint tables are commonly used as guidelines for the interpretation of antimicrobial susceptibility testing results. These are updated annually to reflect new and revised antimicrobial susceptibility breakpoints. EUCAST v.12.0, which was published in January 2022, presents updated meropenem-vaborbactam breakpoints for Enterobacterales and Pseudomonasaeruginosa. It also suggests new breakpoints of susceptibility to various antibiotics for Vibrio spp. Flow charts were updated for Streptococcus pneumoniae and Haemophilus influenzae, and the breakpoints for anaerobic bacteria were divided according to each species. Furthermore, recommendations were made for cases without antimicrobial susceptibility testing breakpoints and links to several rationale and guidance documents were provided for technical convenience.
Antimicrobial susceptibility testing, Breakpoint, EUCAST v.12.0
현재 국내에서 사용되고 있는 대표적인 항균제 감수성 검사의 판독 가이드라인은 Clinical Laboratory Standard Institute (CLSI)와 European Committee on Antimicrobial Susceptibility Testing (EUCAST) 지침으로 각 균종별 새로운 항균제의 해석기준을 포함하여 새롭게 추가되거나 변경되는 내용에 대하여 매년 갱신되어 발표되고 있다. EUCAST는 European Society of Clinical Microbiology and Infectious Disease (ESCMID), European Centre for Disease Prevention and Control (ECDC)와 각 유럽 국가 해석기준 위원회가 공동으로 조직한 상임 위원회로 1997년에 설립되었다. EUCAST 해석기준은 CLSI와 달리 항균제 감수성 검사의 해석기준에 있어서 중등도 내성의 해석기준 없이 내성과 감수성의 해석기준만을 제시하고 있으며, 해마다 갱신되는 내용을 포함하여 균종별 전체적인 해석기준과 관련된 모든 근거 문서를 홈페이지를 통해 무료로 제공하고 있다[1]. 2022년에는 EUCAST v.12.0이 발표되었으며 본문에서는 이번 개정에서 새롭게 추가되거나 변경된 내용에 관하여 다루고자 한다.
2022년 개정된 EUCAST v.12.0 지침에서는 전체적인 내용에서의 주요 변경 사항은 없으나 일부 해석 부분과 기술적인 편의 부분이 추가되었다. EUCAST는 균종별로 각각 항균제 감수성 검사 해석기준표의 상단에 배지, 배양조건, 접종량 및 정도관리 균주의 정보를 포함하는 액체배지 미량희석법이나 디스크 확산법의 방법론을 기술하고 있다. 이번 개정에서는 액체배지 미량희석법의 기술 부분에 최소억제 농도에 관한 추가 정보 확인을 위해서는 EUCAST reading guide를 참고하라는 설명이 추가 기술되었다. 또한 일부 균들의 항균제 감수성 검사에 있어서는 정도관리 균주에 관한 기술부분에 추가적으로 beta-lactam 억제제 성분의 정도관리를 위해서 EUCAST QC표를 참고할 것을 명시하였다. 용어에 있어서는 선별검사에 대한 정의 및 설명이 갱신되었는데 선별검사는 감수성 혹은 내성을 예측하는 한가지 항균제를 사용하고 이는 각각의 항균제를 검사하는 것보다 종종 더 민감하거나 강력할 수 있으며 여러 약제에 대한 감수성 및 내성을 예측할 수 있어서 1차 감수성 검사에서 필요한 검사의 수를 줄일 수 있음을 기술하였다. 선별검사 음성은 해당 항균제 등급에 내성 기전이 없고 최소억제농도(minimal inhibitory concentration, MIC) 값이 감수성 해석기준 이하이거나 억제대의 직경이 감수성 해석기준 이상임을 뜻하고 선별검사 양성은 이와 반대되는 경우이다. 또한 제공되는 EUCAST v.12.0 파일 내에는 선별 항균제명에 링크를 연결하여 이에 관한 지침 문서를 홈페이지에서 확인할 수 있도록 하였다. 또한 기존 일부 항균제에 적용되었던 해석기준에 관한 근거문서 링크를 cefiderocol, imipenem-relebactam, meropenem-vaborbactam, delafloxacin, bedaquiline과 delamanid에도 추가하여 필요 시 찾아볼 수 있도록 하였다.
EUCAST v.12.0에서는 해석기준값에 괄호가 표기된 것(breakpoint in brackets)을 볼 수 있으며 이번 개정에서는 이에 대한 설명이 갱신되었다. 괄호 내의 해석기준값은 표현형으로 검출 가능한 내성 기전이 있는 분리주와 없는 분리주를 구분할 수 있는 기준이다. 이는 역학적인 기준치(epidemiological cut-off)에 근거하는 값으로 이러한 항균제의 단독요법 사용에 대한 임상적인 근거는 부족하다. 하지만 특정 적응증이나 다른 약제와의 병합요법에 대해서는 여전히 사용될 수 있으며 이 해석기준을 적용하여 결과를 보고하고자 할 때에는 내성이 있는 균주는 내성(resistance, R)으로 보고할 수 있으나 만약 감수성(susceptible, S) 또는 중등도 내성(intermediate, I)을 보고할 때에는 이러한 주의사항을 설명할 것을 명시하고 있다.
EUCAST v.12.0에서 새롭게 추가된 해석기준은 carbapenem과 cyclic boronic acid β-lactamase inhibitor병합제제인 meropenem-vaborbactam에 대한 디스크 확산법 해석기준으로, 이는 Enterobacterales, P. aeruginosa에서 Table 1과 같이 적용되었다.
Table 1. New meropenem-vaborbactam breakpoints in Enterobacterales, P.aeruginosa
| Organism | Breakpoint | S ≥ | R < | ATU |
|---|---|---|---|---|
| Enterobacterales | Zone diameter (mm) | 20 | 29 | 15-19 |
| P. aeruginosa | 14 | 14 | – |
Abbreviations: S, susceptible; R, resistance; ATU, area of technical uncertainly .
ATU의 값은 판독 기준은 아니며 해당 결과값이 나올 경우 검사자에게 판독이 어려울 수 있는 범위 내에 있음을 알려주는 경고로 생각할 수 있다. 따라서 ATU 값에 속하는 경우 검사의 불확실성이나 내재적으로 불가피한 변이 요소 등으로 인하여 판독이 어려운 수치에 속한다는 의미로, 필수적인 조치는 없으나 이를 다른 검사법으로 검증하거나 일종의 경고와 함께 보고할 수 있으며 혹은 감수성 여부를 보고하지 않을 수도 있다. Enterobacterales에서는 meropenem-vaborbactam ATU에 해당하는 균주에 대해서는 meropenem에 내성인 경우 meropenem-vaborbactam도 내성으로 보고하고 meropenem에 내성이 아닌 경우에는 추가적인 검사가 필요하다는 부연 설명을 함께 명시하였다.
이번 개정에서 새로운 해석기준표를 도입한 균종은 혐기성균과 Vibrio spp.이며 혐기성균의 경우 기존에는 종별 기준 없이 그람 음성 및 그람 양성균으로만 구분하여 해석기준표를 제시하였으나 EUCAST v.12.0에서는 개별 균종 Bacteriodes spp., Prevotella spp., Fusobacterium necrophorum, Clostridium perfringens, Cutibacterium acnes, Clostiridiodes difficile에 대한 해석기준표를 제시하고 있다. 각 균종별 해당 항균제의 종류는 Table 2와 같다.
Table 2. New EUCAST v.12.0 clinical breakpoint organism-antimicrobial agent for anaerobic bacteria
| Organism | Antimicrobial agent |
|---|---|
| Bacteroides spp. | Piperacillin-tazobactam, Meropenem, Clindamycin, Metronidazole |
| Prevotella spp. | Benzylpenicillin, Piperacillin-tazobactam, Meropenem, Clindamycin, Metronidazole |
| F. necrophorum | Benzylpenicillin, Piperacillin-tazobactam, Meropenem, Clindamycin, Metronidazole |
| C. perfringens | Benzylpenicillin, Piperacillin-tazobactam, Meropenem, Vancomycin, Clindamycin, Metronidazole |
| C. acnes | Benzylpenicillin, Piperacillin-tazobactam, Meropenem, Vancomycin, Clindamycin |
| C. difficile | Vancomycin, Metronidazole, Fidaxomicin |
Abbreviation: EUCAST, European Committee on Antimicrobial Susceptibility Testing.
Vibrio spp.의 경우 해석기준을 적용가능한 균주는 V. alginolyticus, V. cholerae, V. fluvialis, V. parahaemolyticus과 V. vulnificus이며 해당 항균제는 piperacillin-tazabactam, cefotaxime, ceftazidime, meropenem, ciprofloxacin, levofloxacin, pefloxacin, azithromycin, erythromycin, doxycycline, tetracycline, trimethoprim-sulfamethozaxole이다.
Enterobacterales, Pseudomonas spp., Acinectobacter spp.의 colistin에 대한 액체배지 미량 희석법 해석기준에 있어는 역학적 기준치를 근거로 하는 괄호가 삽입되었으며 내성 이외의 값에 대해서는 본문에서 언급한 바와 같이 보고 시 주의를 요한다. 각 균종별 개정된 해석기준과 ATU 값은 Table 3과 같다.
S. pneumoniae의 beta-lactam제제 내성에 대한 oxacillin 선별검사 flow chart는 이전보다 간단하게 변경되고 일부 내용이 갱신되었다. Oxacillin 선별검사에서 beta-lactam 내성 기전이 검출된다고 의심되는 경우에서(억제대 크기 < 20 mm 혹은 MIC > 0.06 mg/L) 억제대의 크기에 따라 해석의 방향이 달라질 수 있으며 이를 나뉘는 기준이 기존 8 mm 미만에서 9 mm 미만으로, 8-19 mm는 9-19 mm로 Fig. 1과 같이 변경되었다.
H. influenzae에서의 beta-lactam제제 내성에 대한 benzylpenicillin 선별검사 flow chart는 기존과 내용상의 변화는 없으나 이전보다 간결한 형태로 변경되었다(Fig. 2).
Table 3. Revised EUCAST v.12.0 clinical breakpoints
| Organism | Antimicrobial agent | S ≥ | R < | ATU |
|---|---|---|---|---|
| P. aeruginosa | Meropenem (indications other than meningitis) | 20 | 14 | – |
| Meropenem (meningitis) | 20 | 20 | ||
| Pseudomonasspp. | Levofloxacin | 50 | 18 | |
| S. epidermidisand S.lugdunensis | Cefoxitin (screen only) | 27 | 27 | 27 |
| S. aureus | Amikacin | (15) | (15) | |
| Coagulase-negative staphylococci | Amikacin | (15) | (15) | |
| Tobramycin | (20) | (20) | ||
| Staphylococcus spp. | Erythromycin (screen only) | 21 | 21 | |
| Clindamycin | 22 | 22 | ||
| Tetracycline (screen only) | 22 | 22 | ||
| Tedizolid | 20 | 20 | 19 | |
| Rimfampicin | 26 | 26 | ||
| Streptococcus group A,B,C, and G | Tetracycline (screen only) | 23 | 23 | |
| Rimfampicin | 21 | 21 | ||
| S. pneumoniae | Ampicillin (indications other than meningitis) | 22 | 19 | |
| Tetracycline (screen only) | 25 | 25 | ||
| Rimfampicin | 22 | 22 | ||
| H. influenzae | Cefotaxime (meningitis) | 27 | 27 | 25-27 |
| Cefotriaxone (meningitis) | 32 | 32 | 31-33 | |
| Tetracyline | 25 | 25 | ||
| M. catarrhalis | Tetracyline | 26 | 26 | |
| B. pseudomallei | Tetracycline (screen only) | 23 | 23 | – |
| Organism | Antimicrobial agent | S ≤ | R > |
|---|---|---|---|
| Pseudomonas spp. | Levofloxacin | 0.001 | 2 |
| S. aureus | Delafloxacin (community-acquired pneumonia) | 0.016 | 0.016 |
| Delafloxacin (skin and skin structure infections) | 0.25 | 0.25 | |
| Amikacin | (16) | (16) | |
| Gentamicin | (2) | (2) | |
| Tobramycin | (2) | (2) | |
| Coagulase-negative staphylococci | Amikacin | (16) | (16) |
| Gentamicin | (2) | (2) | |
| Tobramycin | (2) | (2) | |
| Staphylococcus spp. | Azithromycin | 2 | 2 |
| Erythromycin (screen only) | 1 | 1 | |
| Clindamycin | 0.25 | 0.25 | |
| Tetracycline (screen only) | 1 | 1 | |
| Rimfampicin | 0.06 | 0.06 | |
| Streptococcus group A,B,C, and G | Tetracycline (screen only) | 1 | 1 |
| Rimfampicin | 0.06 | 0.06 | |
| S. pneumoniae | Ampicillin (indications other than meningitis) | 0.5 | 1 |
| Tetracycline (screen only) | 1 | 1 | |
| Rimfampicin | 0.125 | 0.125 | |
| H. influenzae | Cefotaxime (meningitis) | 0.125 | 0.125 |
| Cefotriaxone (meningitis) | 0.125 | 0.125 | |
| Tetracyline | 2 | 2 | |
| M. catarrhalis | Tetracyline | 2 | 2 |
The revised part is indicated in bold type. Breakpoints in brackets are based on epidemiological cut-off. Abbreviations: EUCAST, European Committee on Antimicrobial Susceptibility Testing; ATU, area of technical uncertainly; S, susceptible; R, resistance; MIC, minimal inhibitory concentration.
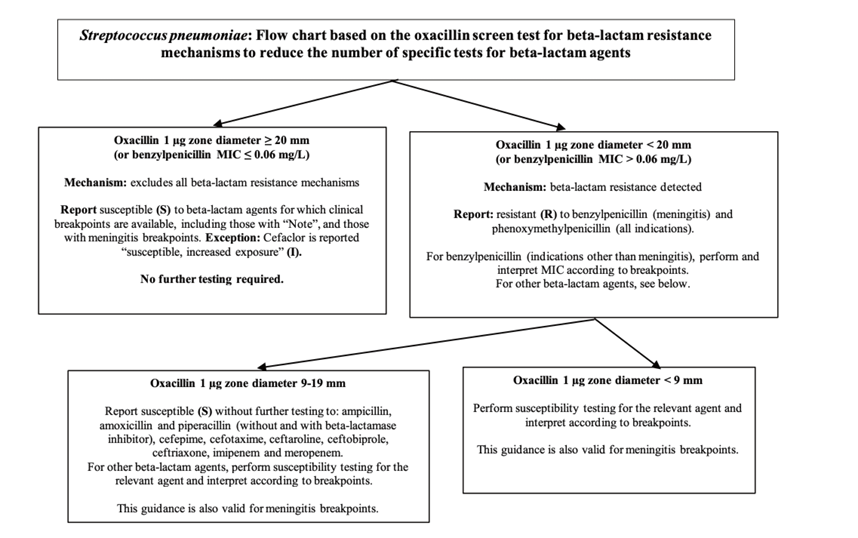
Fig. 1. Flow chart based on the oxacillin screen test for S.pneumoniae. MIC, minimal inhibitory concentration (This figure has been produced in part under ECDC service contracts and made available by EUCAST at no cost to the user and can be accessed on the EUCAST website www. eucast.org.)
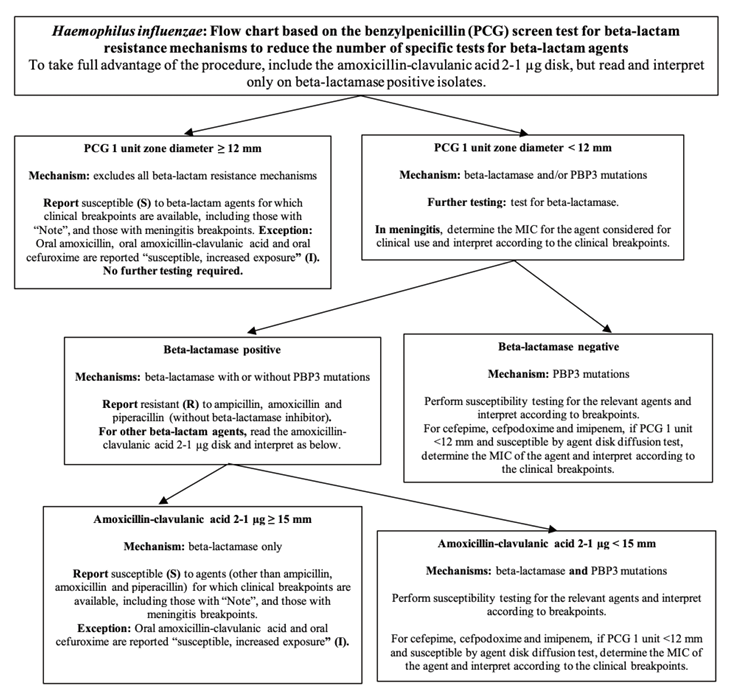
Fig. 2. Flow chart based on the benzylpenicillin screen test for H. influenzae (This figure has been produced in part under ECDC service contracts and made available by EUCAST at no cost to the user and can be accessed on the EUCAST website www.eucast.org.)
2022년 개정된 EUCAST v.12.0 지침에서는 새롭게 추가된 Vibrio spp. 해석기준과 혐기성균의 개별균종에 대한 해석기준을 포함하여 여러 균종별 해석기준값이 갱신되었으며, meropenemvaborbactam에 대한 디스크 확산법 해석기준도 추가되었다. 또한 선별검사에 대한 권장 사항 및 진행 등에 대한 내용과 항균제 감수성 해석기준이 없는 경우에 취할 수 있는 조치에 대한 지침에 대해서도 기술하고 있다.
항균제 감수성 검사의 해석지침으로는 현재 CLSI와 EUCAST의 해석기준표를 주로 이용하며 이는 매년 새로운 항균제 및 해석기준을 제시하고 내용을 갱신하고 있다. 2022년 새롭게 발표된 EUCAST v.12.0에서는 Enterobacterales, P. aeruginosa에서 meropenem-vaborbactam에 대한 해석기준을 제시하고 있으며 기존에 없었던 Vibrio spp.에 대한 항균제의 해석기준을 명시하였다. 또한 S. pneumoniae와 H. influenzae의 선별검사 해석 흐름도를 갱신하였으며 혐기성균의 해석기준을 종별로 구분하여 기술하였다. 그 밖에도 항균제 감수성 검사에서의 해석기준이 명확히 없는 경우 등의 조치를 제시하고 기술적 편의를 위한 지침 내에서의 일부 근거문서 연결 링크도 삽입되었다.
It is not a human population study; therefore, approval by the institutional review board or the obtainment of informed consent is not required.
No potential conflicts of interest relevant to this article were reported.
None.